El diagnóstico mediante imágenes constituye un de los métodos más empleados en la determinación del origen, condición y/o evolución de una enfermedad. Este método se basa en el empleo de diversas sustancias que facilitan la formación de las imágenes, gracias al empleo de dispositivos más o menos complejos.
RADIOGRAFIA (RAYOS X)
Los rayos X son un tipo de radiación altamente energética, de carácter ionizante. Son empleados en medicina para obtener imágenes de los órganos internos y de los vasos sanguíneos.
Cuando un cuerpo o una parte de él es sometido a una fuente (lámpara) de rayos X, la radiación atraviesa el cuerpo y es detectada mediante una película fotográfica (radiografía), una pantalla especial (radioscopia) o por un ordenador (tomografía computarizada). La radiación interacciona con los tejidos en un grado que está determinado por la energía de la radiación y por la densidad y el tipo predominante de átomos de la zona corporal irradiada. Así, los tejidos menos densos permiten que pase a través de ellos una mayor cantidad de radiación, en tanto que los tejidos más densos, como el óseo, absorben parte de la radiación.
Las posibilidad diagnósticas de los rayos X aumentaron notablemente con el desarrollo de la tomografía computarizada (TC), debido a que ésta presenta una mucho mayor resolución (capacidad para ver pequeñas diferencias en los tejidos). Las imágenes tomográficas son formadas cuando los rayos X pasan a través del tejido procedente de múltiples direcciones, formando un círculo. La información procedente del sistema detector múltiple de rayos X es transmitida a una computadora que construye una imagen virtual digital por medio de una matriz, cada uno de cuyos elementos reciben el nombre de pixel y representan un volumen dado de tejido (voxel). Esta imagen es un tomograma, que representa una imagen generada electrónicamente un plano o «rodaja» del órgano o tejido estudiado.
Medios de contraste radiopacos
El empleo de estas sustancias potencia la utilidad de las técnicas radiográficas y los prodecimientos de tomografía computarizada. Se carecterizan por presentar en su estructura uno o más átomos de elevado número atómico y alta densidad, que actúan absorbiendo los rayos X. Esto resulta determinante en la medida que la densidad de los vasos sanguíneos, aparato digestivo y de los tejidos que los rodean es prácticamente la misma. Por ello, la presencia de un radiopaco en un vaso o en el tracto digestivo absorbe parte de los rayos X, actuando como contraste entre el vaso y los tejidos circundantes. La mayor parte de los contrastes radiopacos pueden ser empleados en tomografía compuratizada (TC).
Actualmente, los radiopacos más utilizados son:
– Contrastes baritados: Contienen bario (Ba), con un número atómico (N) de 56 y su peso atómico (pa) es 137,33. Se suelen emplear sales inorgánicas, debido a la prácticamente nula reactividad química del bario, lo que evita que existan efectos biológicos significativos. La sal más utilizada es el sulfato (SO4Ba).
– Contrastes iodados: Contienen uno o varios átomos de iodo (I), con N=53 y pa=126,90. Suele formar parte de moléculas orgánicas debido a que en esta forma su reactividad química es mínima y, además, permite modular la hidro o liposolubilidad del compuesto y, por ende, su farmacocinética.
Los contrastes baritados siguen siendo útiles en el diagnóstico de una amplia variedad de procesos esofágicos, gástricos e intestinales, aunque su baja sensibilidad (en torno al 66%) limita sus indicaciones en favor de otros procedimientos diagnósticos, como la endoscopia o la medicina nuclear.
Los contrastes iodados son ampliamente utilizados todavía e incluso son empleados en algunas de las nuevas técnicas de visualización, como la tomografía computarizada. Los aspectos más importantes relacionados con el uso de estos radiopacos son:
– Osmolalidad: Depende del número de partículas presentes en un volumen dado, pero no de su tamaño o peso. Los radiopacos iodados de elevada osmolalidad están asociados con una mayor incidencia de efectos adversos. A su vez, los derivados iónicos (I) (ácidos y sus sales inorgánicas o de meglumina) presentan una mayor osmolalidad que los derivados no iónicos (NI) (alcoholes, amidas, etc). Las moléculas de los iónicos se disocian en dos partículas cuando son disueltos. Este tipo de contrastes iodados tienen una osmolalidad en torno a 1500 mOsm/kg H2O a una concentración de de 280 mg I/ml. Por el contrario, lo no iónicos no son disociables y sólo forman una partícula por molécula cuando son disueltos. Incluso algunos agentes no iónicos son capaces de formar agregados moleculares, que reducen aun más la cantidad total de partículas presentes en la solución y con ello la osmolalidad. Este tipo de agentes presentan unos valores de osmolalidad de 550-900 mOsm/kg H2O a concentraciones de 250-350 mg I/ml.
– Radiodensidad: Depende de la cantidad relativa de iodo presente en cada molécula. La cantidad de átomos de iodo presentes en cada molécula determina la radiodensidad del agente. Los radiopacos iodados de «primera generación» (diatrizoato, iotalamato, metrizoato, etc) tienen un carácter iónico, Por consiguiente, los derivados iónicos (cuyas moléculas se disocian en dos partículas en solución) presentan un índice de iodo/partícula que es la mitad que un contraste de tipo no iónico que tenga los mismos átomos de iodo. Por ejemplo, el ácido ioxáglico tiene 6 átomos de iodo por molécula, pero tiene un carácter iónico (forma dos partículas por molécula en disolución), de ahí que su índice de iodo sea de 6:2, o lo que es lo mismo, 3.
– Viscosidad: Es otro de los factores determinantes de la toxicidad de los radiopacos iodados, ya que afecta al tiempo durante el cual un órgano o vaso está expuesto a los efectos del agente. También es determinante para la facilidad y rapidez de la administración del contraste. Una elevada viscosidad puede resultar problemática, especialmente cuando se emplean catéteres de pequeño calibre interior. La viscosidad está relacionada con el tamaño de partícula. De ahí que los contrastes que forman agregados moleculares tienden a tener una mayor viscosidad.
Salvo para indicaciones muy específicas (urografía, colangiografía), el contraste iodado ideal es aquel con el mayor cociente Radiodensidad/Osmolalidad.
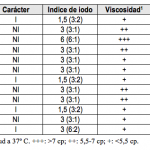
TABLA 1. CARACTERÍSTICAS DE LOS RADIOPACOS IODADOS
Indicaciones de los contrastes radiopacos
– Urografía: Se emplean productos con bajo peso molecular e hidrosolubles, y con un bajo índice de unión a las proteínas plasmáticas, con el fin de facilitar la filtración glomerular del contraste y su paso a través del tracto urinario.
– Angiografía: De similares características a los empleados en urografía, salvo en lo relativo a la unión a las proteínas plasmáticas. Es importante que tengan una baja viscosidad para facilitar unainyección intravenosa rápida, así como una elevada radiodensidad para contrarrestar la dilución del contraste en el volumen sanguíneo.
– Radiografía gastrointestinal: Deben ser no obsrbibles por vía oral, capaces de formar un tapiz homogéneo sobre la mucosa digestiva y no interferir con las secreciones intestinales ni producir imágenes radiográficas irreales (artefactos radiográficos). Su prototipo es el sulfato de bario.
– Colecistografía y colangiografía: Si se emplea la vía intravenosa, se prefieren moléculas que presenten en su estructura una función ácida libre, con el fin de potenciar su excreción con la bilis. Esto es debido a que existe un sistema biliar de transporte selectivo de tipo aniónico específico para ácidos orgánicos. Se prefieren derivados de alto peso molecular y con elevada tasa de unión a proteínas plasmáticas, con el fin de impedir una excreción renal rápida (acido iotróxico). Por el contrario, en colecistografía oral se requieren moléculas pequeñas, suficientemente solubles en los fluidos gastrointestinales y suficientemente lipófilas como para difundir a través de las membranas de la mucosa (ácido iopanoico). Se suelen administrar conjuntamente con comidas extragrasas.
– Mielografía: Los contrastes radiológicos para médula espinal no requieren nada especial, aunque habitualmente son empleados derivados hidrosololubles de carácter no iónico como iotrolán.
Efectos adversos de los contrastes radiopacos
En principio, los contrastastes baritados no plantean problemas de toxicidad, dada la prácticamente nula absorción del bario en el aparato digestivo. No ocurre lo mismo con los contrastes iodados, que presentan un perfil toxicológico nada desdeñable. En la tabla 2 se especifica la clasificación la gravedad de los efectos adversos.
TABLA 2. TOXICIDAD DE LOS CONSTRASTES IODADOS
| Nivel de gravedad | Efectos adversos |
| Leve | Náuseas, vómitos leves, urticaria limitada, sensación de calor, rubefación, prurito, palidez, dolor en el punto de inyección, arritmias cardíacas transitorias (contracciones ventriculares prematuras aisladas). |
| Moderado | Vómitos intensos, edema en la cara y/o faringe, broncoespasmo, disnea, escalofríos, dolor torácico y/o abdominal, cefalea. |
| Grave | Síncope, convulsiones, edema pulmonar, shock, arritmias cardíacas graves (taquicardia ventricular), parada cardiorrespiratoria. |
Hay estudios que permiten afirmar que los radiopacos iodados de baja osmolalidad presentan una incidencia menor de efectos adversos leves o moderados que los de elevada osmolalidad. Sin embargo, esto mismo no ha podido ser demostrado para los efectos más graves.
Las reacciones de origen alérgico son más comunes con los agentes iónicos que con los no iónicos de menor solubilidad. Los pacientes con mayor riesgo de padecer este tipo de reacciones son aquellos con historial de asma, alergia a medicamentos, supresión adrenal, enfermedades cardíacas, reacciones anteriores a medios de contraste y aquellos tratados con betabloqueantes o interleucina 2 (aldesleucina). En este tipo de pacientes son preferibles los agente de tipo no iónico.
Los medios de contraste de tipo no iónico tienen, por otra parte, una mayor capacidad agregante plaquetaria que los iónicos, lo que redunda en un mayor potencial trombogénico.
RESONANCIA NUCLEAR MAGNÉTICA (RNM)
Esta técnica de visualización no requiere ningún tipo de radiación ionizante, sino someter al paciente a un intenso campo magnético que provoca un alineamiento en la misma dirección de los núcleos de los átomos de hidrógeno del organismo, que se comportan como dipolos magnéticos. Mientras el campo magnético se mantiene, el paciente recibe una radiación de origen múltiple y de baja energía (radiofrecuencia) que es absorbida por los núcleos de hidrógeno, haciéndolos vibrar en una dirección diferente de su posición original.
Cuando se suspende la radiofrecuencia, los núcleos de hidrógeno vuelven al alineamiento original producido por el campo magnético. Este cambio de alineación va acompañado por la emisión de una señal que es detectada e interpretada mediante un ordenador, el cual construye una imagen virtual basándose en la distribución y concentración de los núcleos de hidrógeno en el tejido u órgano analizado.
Dado que el hueso tiene una proporción baja de átomos de hidrógeno en relación al resto de los tejidos (predominan los átomos de calcio), no interfiere en las imágenes de los tejidos blandos. El resultado es la producción de imágenes anatómicas de alta resolución, siendo una técnica especialmente utilizada para exploraciones neurológicas, musculares y articulares, aunque la amplitud de sus indicaciones diagnósticas crece día a día, a medida que se abaratan el coste de los complejos equipos necesarios.
La RNM también emplean sustancias para mejorar la calidad de la información anatómica conseguida. No se trata de contrastes al estilo de la radiografía, sino agentes conteniendo átomos paramagnéticos (hierro, manganeso, gadolinio, etc), que alcanzan un momento magnético relativamente grande al ser sometidos a un campo magnético. Esto afecta a la respuesta de los núcleos de hidrógeno de los átomos de agua próximos al agente paramagnético e incrementa la señal, mejorando aun más la calidad de la información. La preparación de diversos derivados permite disponer de agentes específicos para determinados órganos y/o tejidos (hígado, cerebro, corazón, etc).
La RNM ha sustituido en gran medida a la tomografía computarizada en el diagnóstico de la mayoría de los procesos tumorales, inflamatorios o degenerativos, aunque la tomografía sigue teniendo por ahora un utilidad incuestionada en el diagnóstico de procesos agudos (hemorragias, traumatismos, etc).
TABLA 3. POTENCIADORES DE CONTRASTE PARA RNM
| Átomo
paramagnético |
Derivado | Comentarios |
| Gadolinio (Gd) | Acido Gadopentético Gadodiamida | El ácido gadopentético es el agente de referencia de los contrastes para RNM con gadolinio. Presenta una elevada osmolalidad (2000 mOsm/kg H2O). Gadodiamida presenta una baja osmolalidad (menos de la mitad que la del ácido gadopentético y sus sales).debido a que tiene una naturaleza no iónizable, por lo que en disolución cada molécula da lugar a una sóla partícula. |
| Acido Gadotérico Gadoteridol | La menor osmolalidad de estos derivados, en especial el gadoteridol, en relación al ácido gadopentético, les confiere la teórica superioridad de ser mejor tolerados por los pacientes. | |
| Hierro (Fe) | Ferumóxidos | Constituyen una forma de partículas cristalinas superparamagnéticas de óxido ferrroso-férrico, estabilizadas con dextrano de bajo peso molecular. Se utilizan específicamente en el diagnóstico de tumores abdominales y de la pelvis, debido a que estas partículas son selectivamente fagocitadas por las células del sistema reticuloendotelial en órganos como el hígado, el bazo y la médula ósea. Dado que las células tumorales carecen de capacidad fagocítica, las imágenes por RNM se obtienen por contraste con los tejidos sanos. |
| Hierro (III), Oxido | Características y aplicaciones diagnósticas similares (cáncer de hígado). | |
| Manganeso (Mn) | Mangafodipir | Se trata de un complejo de manganeso con dipiridoxal difosfato (DPDP), con el fin de reducir la toxicidad intrínseca del manganeso. Este ligando es utilizado para que sea reconocido por el sistema de transporte de membrana para la vitamina B6 (piridoxina) de los hepatocitos. Esto justifica la selectividad y alta tasa de retención hepática del mangafodipir, que permite diferenciar los tumores hepatocelulares (carcinomas hepatocelulares) de aquellos que no tienen un origen hepatocelular. |
ULTRASONIDOS (ECOGRAFÍA)
El diagnóstico por imágenes basado en ultrasonidos se basa en un principio bastante simple. Un dispositivo transductor emite una ondas de ultrasonido que son reflejadas (eco) por los tejidos y órganos, siendo recuperadas por el transductor. Con esa información del eco recibido, un ordenador se encarga de construir una imagen virtual, que puede ser reproducida en un papel o en un monitor de televisión.
En general, la calidad de la imagen es inferior a la RNM y a la TC, pero tiene dos grandes ventajas. La primera es la de ser una técnica bastante incocua para el paciente, especialmente en obstetricia, donde se ha convertido en una técnica diagnóstica de primera línea. La segunda consiste en que los equipos son notoriamente más baratos que los de RNM y TC.
Existen algunas modalidades que han ampliado los horizontes diagnósticos de esta técnica, como la ecografía de efecto Doppler. Esta se basa en el conocido principio físico que lleva tal nombre y que implica la existencia de un cambio en la frecuencia del sonido cuando es reflejado por un cuerpo en movimiento. En esta técnica, el haz ultrasónico (de una frecuencia inicial conocida) es reflejado por un elemento móvil, como es la sangre dentro del corazón y de los vasos. El Eco-Doppler es muy usado en el estudio de la integridad y funcionalismo vascular (extremidades, abdomen, cuello, etc).
También se emplean ciertos agentes con el fin de incrementar la utilidad de las imágenes ecográficas y hacer exploraciones selectivas de ciertos órganos y tejidos. En este sentido, ha alcanzado un especial desarrollo la ecocardiografía, así como la ecografía de abdomen y de pequeños órganos superficiales (tiroides, testículos, parótidas).
Uno de los más empleados es la asociación de ácido palmítico/galactosa, usada en ecocardiografía. Más modernas son las microsferas de albúmina humana. Se trata de un preparado de albúmina humana tratado térmicamente, que conduce a la formación de unas microesferas de un diámetro medio entre 2,5 y 4 µm, que contienen octafluoropropano. Este último es responsable de la generación de potentes ecos, claramente distinguibles de los procedentes de los tejidos humanos blandos, que además son potenciados por las propias microesferas de albúmina. Este preparado es utilizado en ecocardiografía, permitiendo la opacificación ecográfica de las cámaras cardíacas y la visualización de los movimientos de las paredes y del flujo sanguíneo cardíacos.
El contenido aquí mostrado corresponde a BOT (base de datos de medicamentos en España 2002), que aunque está relacionado con medicamentos de uso humano, puede resultar muy útil para la medicina veterinaria de pequeños animales.

 Campus Virtual del Hospital Veterinario J. Griñán
Campus Virtual del Hospital Veterinario J. Griñán